
鉄は錆びて当たり前!でも、なんで錆びるのでしょう?
そのメカニズムと錆を防止できる方法を今回はお伝えします。
1、鉄について
1−1、鉄の利用価値
そもそも金属というのは自然界の鉱石から人為的に作られた物で、その中でも鉄は、どの天体にも存在しているくらい豊富にあります。安くて入手しやすく、比較的加工もやりやすいので、いろんな所で利用されている利用価値の高い金属です。例えば、毎朝通期で利用している車や電車のボディー、車などで道路を走っている時に目にする信号機や標識やガードレール、電車が走るために必要なレール、缶コーヒーなどを買うための自動販売機などなど、みなさんの生活の中でも必ずどこかに使われていますよね。
1−2、鉄は元素
鉄は、原子番号26番で、元素記号Feで表せれる金属元素です。鉄鉱石を精錬する事で鉄は生産され、鉄は合金として加工される事によって、いろんな特徴を持った金属に変化する事ができます。
2、なぜ錆びるのか?
2−1、原子・分子・電子について
原子とは、最も小さい粒のことです。その原子同士がくっついているのを分子と呼び、それをくっつける役目を持ったものが電子です。分子は電子をちょっと多く持ったり少なく持ったりできます。多いのが「マイナスイオン」、少ないのが「プラスイオン」と呼ばれます。ちょうどいい数の電子を持っている状態が一番安定している状態なのです。例えば、静電気ってありますよね?あの「パッチ!」っていうやつです。あれは、電子が移動して起こる現象なんですよね。
2−2、イオン化現象
鉄は、雨などの自然環境で水に濡れると、表面についた水分が鉄を溶解しイオン化しだします。つまり、ちょうどいい数の電子を保持しているのを邪魔され、イオン化現象が始まります。
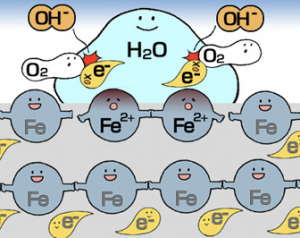
水分は、空気中の酸素と溶け込み、鉄から電子を奪い「水酸化鉄イオン」になります。また、鉄は、電子を奪われてしまったため、「Fe2+」という「鉄イオン」になります。その鉄イオンからさらに電子がなくなり、Fe2+が「Fe3+」に変化します。
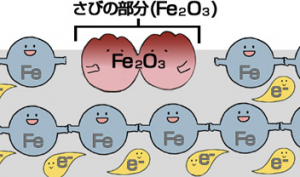
Fe3+は水分によって発生した水酸化鉄イオンを引き寄せ、その後水分がなくなり、「酸化鉄」というサビになるのです。これが、鉄が錆びるメカニズムです!
3、錆の予防方法
3−1、塗装

鉄の表面に錆止め塗料などを塗って、Feの分子たちを酸素や水などから邪魔されないように閉じ込める。錆止めの塗料は、灰色や赤茶色などの地味な色しかありませんので、錆止め塗料を塗った後に、お好みの色で上塗りしましょう!
3−2、メッキ処理

これは専門の業者に頼まないと難しいかもしれませんが、酸化しにくい金属で表面を覆い保護する方法です。亜鉛メッキが代表的ですが、めっき液が入った大きな曹に鉄を浸け込み、その曹に電気を流して電気の力で鉄の表面に亜鉛を付着させます。メッキ処理してから塗装すると、これは合わせ技の最強コンビですね。
まとめ
鉄はとにかく加工がしやすく、様々な物に変化できる魅力的な金属です。北京オリンピックの頃に鉄の値段が高騰し、公園の滑り台や水道の蛇口や側溝の蓋などの盗難被害があっていたのがまだ記憶に新しいですが、それくらい身近に存在する金属という事なんです。鉄は結構暖か味のある素材です。きちんと手入れをして錆びさせないようにしてください。
弊社は、
そんな金属を加工することを得意としている会社です!
「こんなの作って欲しい」「こんなの作れますか?」などなど、








この記事へのコメントはありません。